Kolmest jääb väheks: benseeni elektronstruktuur eksisteerib mitte vähem kui 126 mõõtmes!
Ligi 200 aastat pärast seda, kui Michael Faraday benseeni molekuli avastas, on teadlastel viimaks õnnestunud kirjeldada selle keerukat elektronstruktuuri.
Lisaks 1930. aastatest peale tuurinud debati lahendamisele on avastus oluline ka järelmite poolest optoelektrooniliste materjalide arendamisele tulevikus, kuna paljud neist konstrueeritakse just benseenidest.
Benseeni aatomstruktuuri mõistavad teadlased üsna hästi — see on kuuest süsinikuaatomist koosnev võru, mille iga süsinikuaatomi külge kinnitub üks vesinikuaatom.
Kui aga võtame arvesse molekuliga seotud 42 elektroni, muutub pilt äärmiselt tüsilikuks.
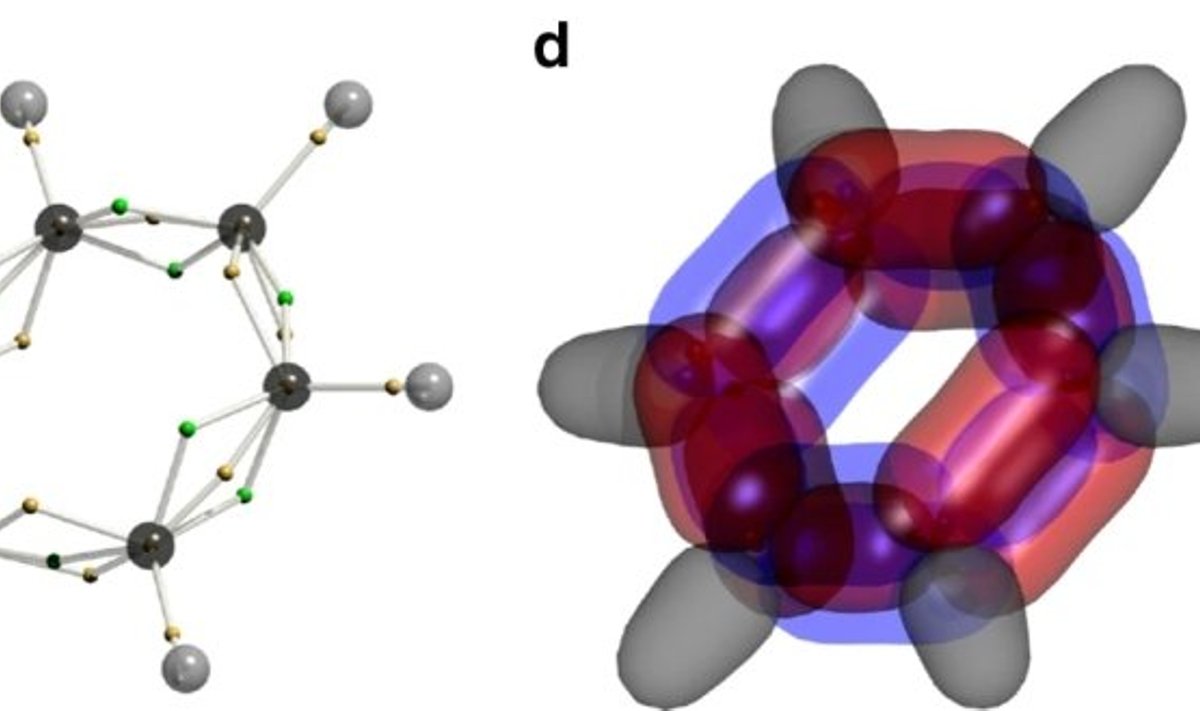
„Benseeni elektrone kirjeldaval matemaatilisel funktsioonil on 126 mõõdet,“ selgitas Uus-Lõuna-Wales'i ülikooli UNSW juures tegutseva Austraalia teadusnõukogu eksitoniuuringute kompetentsikeskuse (ingl ARC Centre of Excellence in Exciton Science) ja UNSW Sidney keemik Timothy Schmidt.
„See tähendab, et funktsioonil on 126 koordinaati — kolm koordinaati iga elektroni jaoks. Need elektronid pole sõltumatud, mistõttu ei saa me funktsiooni taandada 42 sõltumatuks kolmemõõtmeliseks funktsiooniks. Arvutiga kalkuleeritud lahendit on inimestel keeruline tõlgendada, mistõttu pidime välja mõtlema uue viisi vastuse saamiseks,“ ütleb ta.
Benseeni elektronstruktuuri matemaatilisel kirjeldamisel tuleb arvesse võtta 126 mõõdet. Just taolise keerukuse tõttu on struktuuri väljaselgitamine nii pikka aega ebaõnnestunud ja toonud kaasa vaidluseid teemal, kuidas benseeni elektronid tegelikult käituvad.
Välja on kujunenud kaks selgelt eristuvat mõttesuunda. Ühe kohaselt järgib benseen valentssidemete teooriat, milles elektronid on lokaliseeritud; teise kohaselt kehtib benseeni puhul molekulaarorbitaalide teooria, milles elektronid on delokaliseeritud. Probleem seisneb eelkõige selles, et kumbki teooria ei paista paika pidavat.
Schmidti ja kolleegide töörühma uurimus rajaneb hiljuti nende endi välja töötatud tehnikal, mis rakendab algoritmilist lähenemist mitme elektroniga süsteemi lainefunktsioonide visualiseerimisele.
„Sisuliselt ühendab see keemilise mõtlemise näidates, kuidas kaks benseeni kirjeldamisel kasutatavat valitsevat paradigmat on võimalik ühildada,“ rõhutas Schmidt.